96
молекулой цинка происходит атака атомов Н на диполь-дипольную связь между
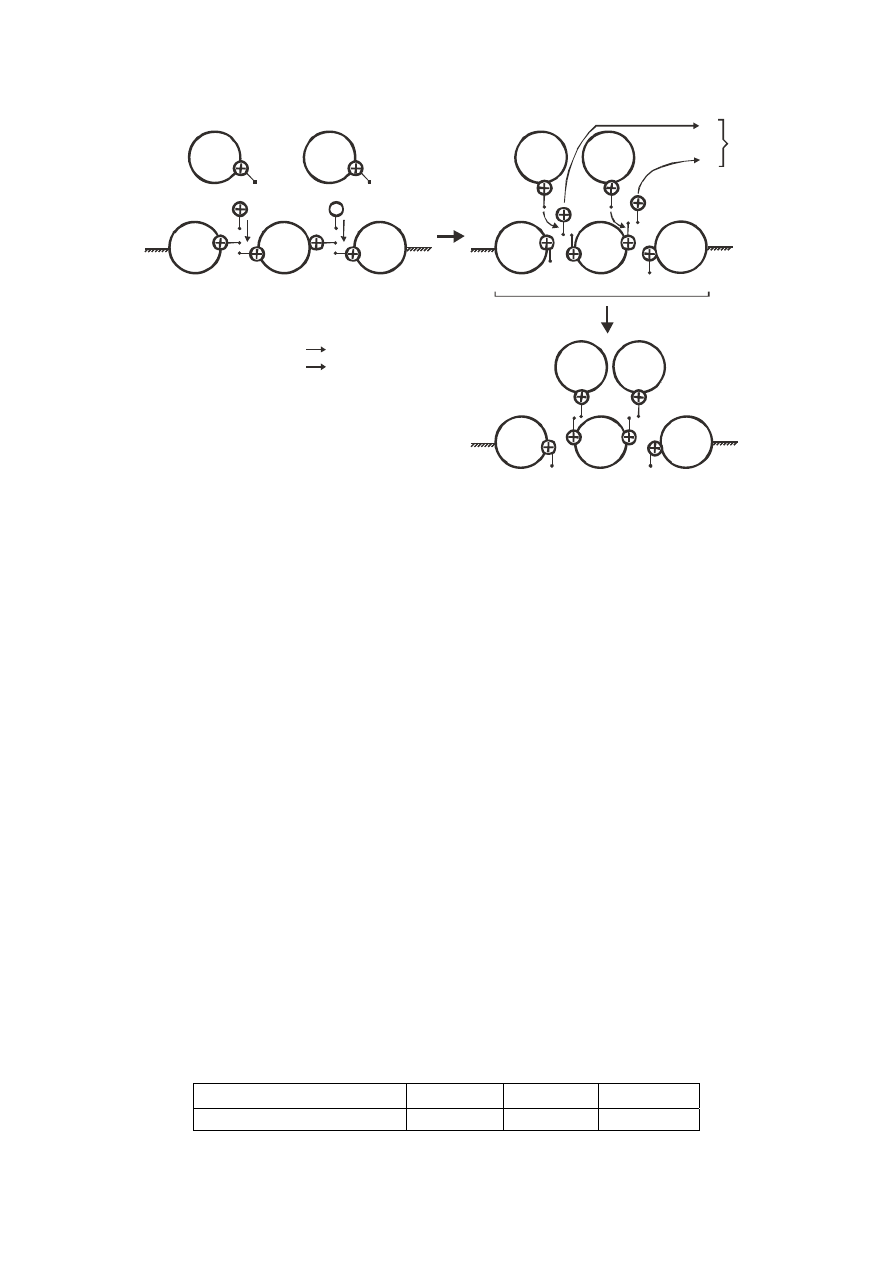
двумя атомами цинка (рис 18).
H
Zn
Zn
H
Zn
+
HOH
Cl
Cl
H
Zn
Zn
H
Zn
H
2
Cl
Cl
Zn
Zn
Zn
Cl
Cl
(Zn-Zn-Zn) + 2Н Zn Н-Zn-Н Zn
(Н-Zn-Н) + 2Cl ZnCl + Н
2 2
Рис. 18. Схема взаимодействия соляной кислоты с цинком.
Образуется новая диполь-дипольная связь Н-Zn-Н и формируется гидрид
цинка Н-Zn. Таким путем атом цинка отделяется от решетки. Далее атомы хлора
вытесняют атомы водорода и занимают их места. Такой обмен обусловлен тем, что
энергия связи Zn-Н составляет всего 19,5 ккал/моль, а энергия связи Zn-Cl
составляет по разным данным от 50 до 70 ккал/моль. Образовалось соединение
ZnCl
2
, а вытесненные два атома водорода через короткий промежуток времени
образуют молекулу Н
2
.
Из
сказанного
выше
следует,
что
растворителем
веществ
или
отделителем атомов друг от друга в любых веществах (соединениях) является
свободный атом водорода, независимо от способа его получения.
Макрокристаллы металлов, в зависимости от количества свободных валентных
диполей на кристаллах атомов, могут иметь на гранях своей поверхности
свободные валентные диполи или не иметь таковых. Так атомы с одним валентным
диполем Cu, Ag и Au образуют двухатомные молекулы и на поверхности
макрокристаллов из этих элементов свободные валентные диполи появиться не
могут; поэтому эти металлы не подвергаются окислению в нормальных условиях.
Атомы, имеющие два и три валентных диполя, например, Mg, Al, Fe, после
формирования из них молекул и далее макрокристаллов, на определенных гранях
будут иметь валентные диполи, выходящие на поверхность, доступные для
адсорбирующихся молекул. Молекулы, имеющие свободные валентные диполи,
такие как, например, парамагнитная молекула кислорода (см. раздел 6) активно
взаимодействует со свободным диполем поверхности металла. В результате такого
взаимодействия образуются оксидные пленки на металлах.
В отличие от всех щелочных металлов три металла Cu, Ag и Au имеют
гранецентрированную кубическую структуру и обладают большой плотностью,
благодаря значительному количеству избыточных нейтронов от 5 до 39 (атомы с
избыточными нейтронами – это атомы у которых отношение протон/нейтрон
1).
Элемент
Cu Ag Au
Удельный вес, г/см
3
9,0 10,5 19,3
Химическая активность меди и ее аналогов сравнительно невелика и по ряду
Cu-Ag-Au быстро уменьшается. Золото и серебро на воздухе не изменяются, а медь