90
HOH+ NaOH
Безводное
соединение NaOH электрического
тока
не
проводит.
Взаимодействие с водой NaOH приводит к растворению последнего, и этот раствор
становится электропроводящим.
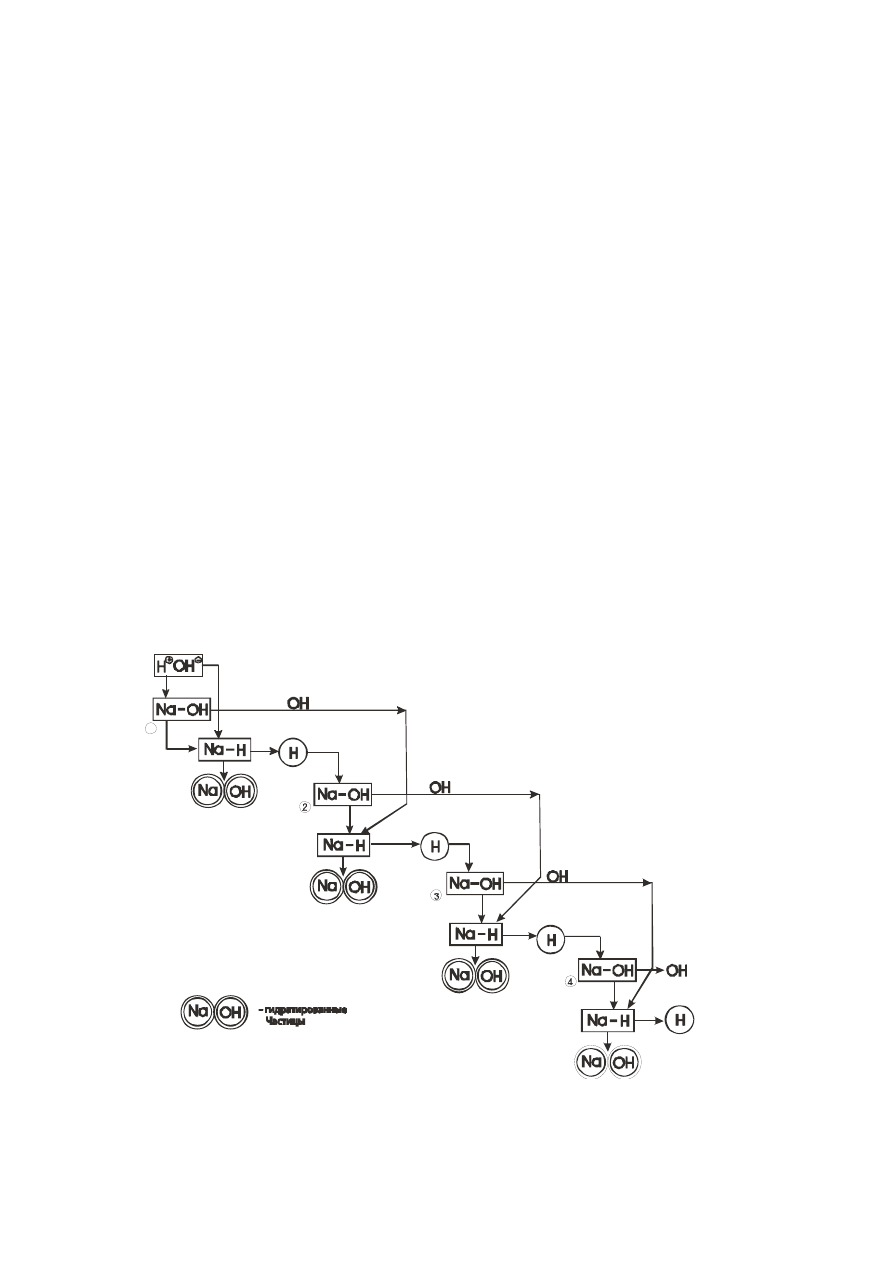
Рассмотрим механизм взаимодействия воды и соединения NaOH. Итак, имеем
одну автодиссоциированную молекулу воды - это атом Н и ОН группа (схема 12).
Первым актом взаимодействия является атака атома Н на связь Na-OH; получаем
гидрид NaH, который по причинам, изложенным выше (при растворении NaCl в
воде) подвергается атаке группы ОН от исходной молекулы воды. В результате
отделяется кислотный атом Н и пара гидратированных частиц - атом Na и группа
ОН. Обе частицы, являясь электрически нейтральными, имеют отрицательную
полярность, то есть обе выполняют функцию основания и они обеспечивают
электропроводимость раствора.
Как видно из схемы 12 эти два типа взаимодействия, атака атомом Н
межатомной связи и последующее вытеснение ОН группой атома Н из гидрида
натрия, приводит к гидроразделению Na и ОН благодаря присутствию квадруполей
на поверхности атомов Na и O, которые способствуют присоединению молекул
воды, с образованием гидратных оболочек. Эта реакция будет продолжаться до
полного растворения всех исходных молекул NaОН. Реакция имеет цепной
характер. Если из раствора NaОН удалить воду, атом Na и ОН группа
восстанавливают между собой диполь-дипольную связь, образуя целостную
молекулу и электропроводность пропадает.
В процессе диссоциации молекул кислот, солей и оснований в определённом
количестве должен выделяться атомарный кислород при расщеплении перекиси
водорода по схеме:
НО+ОН
НОН + О,
которая образовывалась из двух ОН-групп, имеющих отрицательную полярность, и
которые всегда присутствуют в растворах вышеуказанных соединений.
1
(12)
Как видно из таблицы 15 молекулы кислот, содержащие в своем составе атомы
хлора и группы NO
3
и SO
4
(HCl, HNO
3
, H
2
SO
4
) имеют высокую степень
диссоциации благодаря цепным реакциям атома Cl и групп NO
3
и SO
4
с молекулами
воды (схемы реакций для молекул этих кислот аналогичны). Самую малую степень