59
движений, переходят в состояние жидкости. При этом происходит принудительное
уплотнение молекул в единице объёма, что равноценно увеличению массы газа и
это сопровождается увеличением магнетизма этого объёма и усилению его
взаимодействия с магнитным полем Земли, т.е. осуществляется гравитационное
взаимодействие, соответствующее жидкостному фазовому состоянию. Массой пяти
атомов азота М=5х14=70 и четырёх атомов кислорода М=4х16=64, соединённых
треугольной и тетраэдрической связью (табл. 5) соответствуют состоянию
жидкости.
Обратимся к твёрдому телу. Из кристаллохимии известно, что любой кристалл
состоит из элементарных ячеек. Элементарная ячейка - это наименьший возможный
объём пространственной решетки кристалла, отображающий все возможности
структуры.
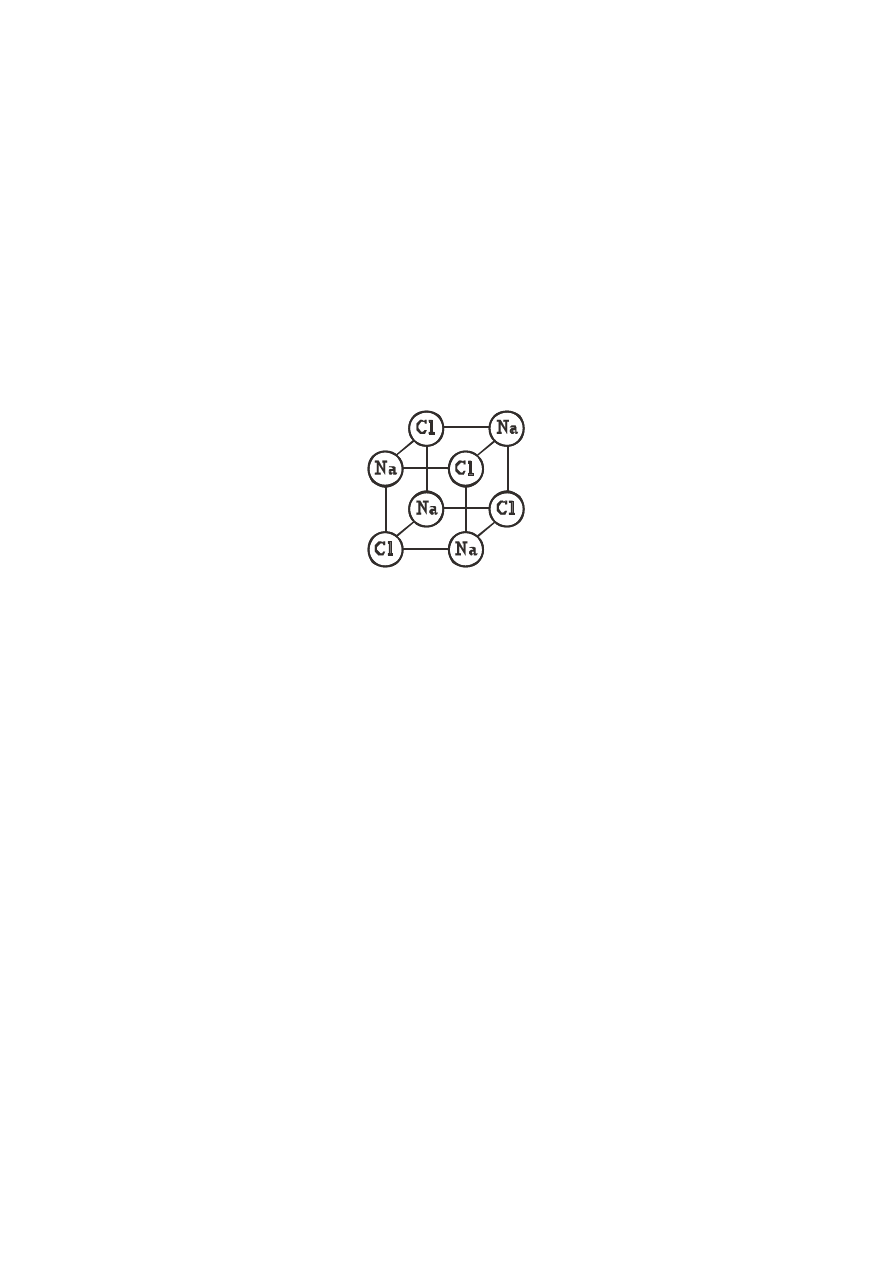
Рассмотрим в качестве примера NaCl. По нашим данным кристалл NaCl
состоит не из ионов Na+ и Cl-, а из молекул Na-Cl [1, 5]. Молекула NaCl имеет
молекулярный вес 23+35=58. Элементарная кубическая ячейка кристалла NaCl
состоит из 4-х молекул NaCl:
Отсюда 58х4=232. Эта величина молекулярной массы, в соответствии с
таблицей соответствует твёрдому телу.
Особый интерес для нас представляют жидкости. Возьмем в качестве примеров
известные
жидкости,
например,
бензол,
уксусную
кислоту,
глицерин.
Молекулярный вес бензола С
6
Н
6
составляет М=78ед.; уксусной кислоты (СН
3
-
СООН)→М=60ед.; глицерина (СН
2
ОН-СНОН-СН
2
ОН)→М=92. Эти цифры попадают
в диапазон молекулярных весов, характерных для жидкости.
Рассмотрим спирты, и в качестве примера возьмем этиловый спирт; его М=46.
Эта величина соответствует газовому состоянию (таблица 8). Однако, всем хорошо
известно, что спирт в нормальных условиях является жидкостью. Какие же силы
способствуют переводу легких молекул спирта в жидкость? Известно, что
молекулы, имеющие в своем составе ОН группы, могут взаимодействовать между
собой с помощью водородной связи (Н-связи). Если соединить две молекулы
С
2
Н
5
ОН водородной связью, то такая структура будет иметь вес М
2
=46+46=92. Эта
величина с учетом данных таблицы 8 соответствует жидкости. Учитывая то, что
каждый атом кислорода может участвовать в образовании двух Н-связей,
определим, сколько же молекул спирта может входить в ассоциат, образованный
химическими Н-связями (Н-ассоциат), чтобы спирт оставался в состоянии
жидкости? Соединим три молекулы спирта – М
3
=46х3=138; эта величина
соответствует жидкости. Четыре молекулы спирта также имеют фазовое состояние
жидкости: М
4
=46х4=184; тогда как 5 молекул попадают в разряд твердого тела:
М
5
=46х5=230. Удерживать пять и более молекул спирта в едином комплексе
энергии Н-связей, по-видимому, недостаточно при нормальных условиях (норм. Т
0
и Р). Тепловые колебания не дают возможности для существования стабильного Н-
ассоциата из 5-6 молекул спирта, и он разрушается.
Рассмотрим в качестве еще одного примера жидкость с названием ацетон.
Молекула ацетона Н
3
С-СО-СН
3
имеет вес М=58, что соответствует фазе газа. Но
ацетон – жидкость. Водородных связей между этими молекулами не может быть,
но имеется атом кислорода, у которого на поверхности присутствуют два