26
Продолжение табл. 3.
1 2
3
4
5
6
7
Al +
1+
1
H
14+
28
Si
14n
(2)
(2)(2)(2)(2) 4
He
14n
8,1
4 валетных
диполя
Si +
1+
3
T
2n
15+
31
P
16n
(2)
(2)(2)(2)(2) (2)3
He
16n
10,5
3 валетных
диполя
1 квадруполь
P +
1+
1
H
16+
32
S
16n
(2)
(2)(2)(2)(2)
(2)(2)2
He
16n
10,3
2 валетных
диполя
2 квадруполя
S +
1+
3
T
2n
17+
35
Cl
18n
(2)
(2)(2)(2)(2) (2)(2)(2)1
He
18n
13,0
1 валетный
диполь
3 квадруполя
Cl +
1+
5
H
4n
18+
40
Ar
22n
(2) (2)(2)(2)(2) (2)(2)(2)(2)
He
22n
15,7
0 валетных
диполей
4 квадруполя
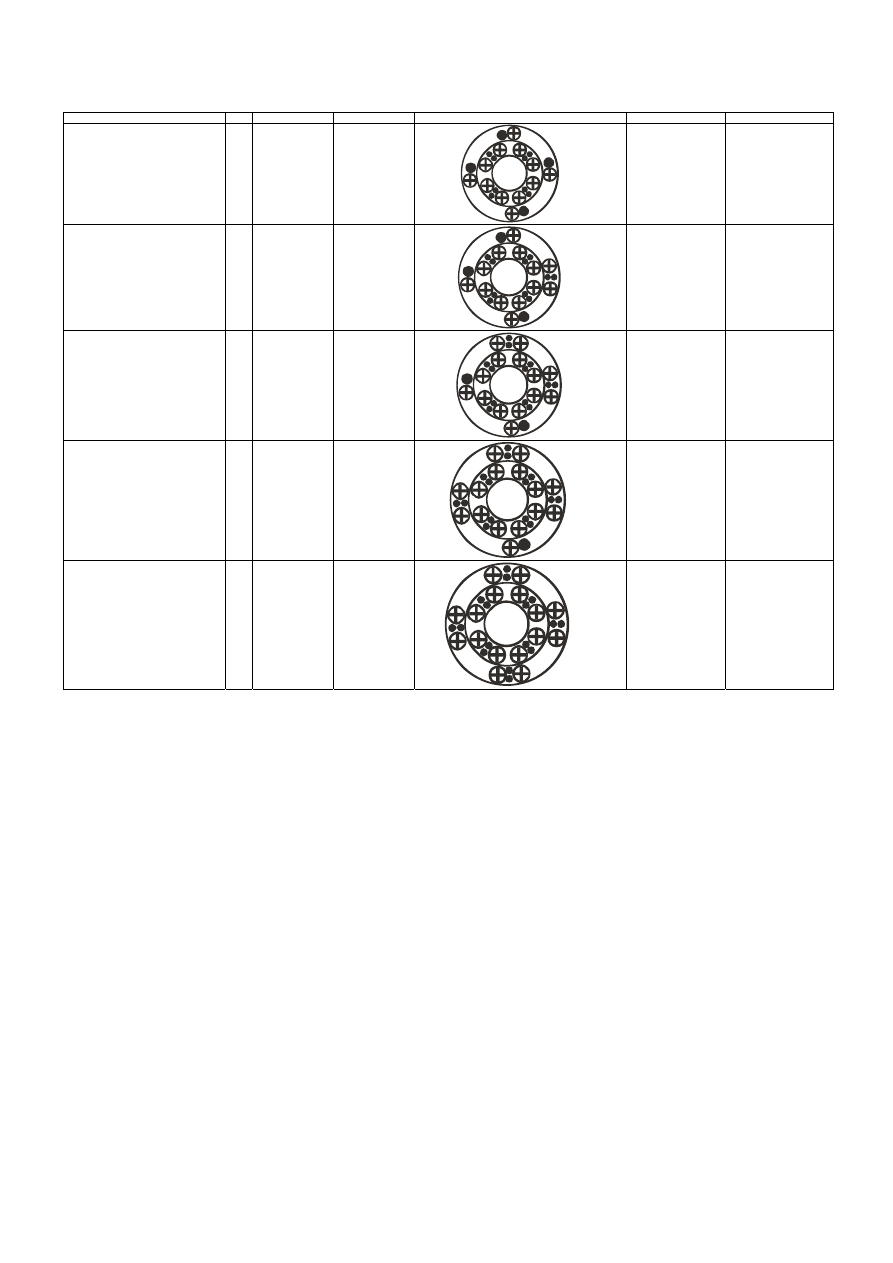
В таблице 3 представлена схема формирования атомов химических элементов
2-го и 3-го периодов. Для атомов 2-го периода все квадруполи L-слоя доступны
для образования химической связи. Для атомов 3-го периода их четырёх
квадруполей L-слоя доступны 2 или 3 квадруполя для образования химических
связей с другими атомами.
Опираясь на модели атома гелия и атома лития, считаем, что атом является
кристаллическим образованием, и он подчиняется закономерностям роста
кристаллов. Затравкой, или центром кристаллизации, для атомов всех химических
элементов является атом гелия, строительным материалом, строительными
кирпичиками является атом водорода и его изотопы. В кристаллах обычно
соблюдается принцип плотнейшей упаковки. Последняя является энергетически
наиболее выгодной, так как приводит к тесному сближению частиц и их наиболее
сильному взаимодействию.
Силы, под действием которых происходит процесс кристаллизации –
увеличение размера и массы кристалла атома – имеют природу электрическую,
магнитную и гравитационную (в нашем обобщенном определении). Имея в виду
свойство пары протон-электрон, то есть атома водорода, и свойства изотопов
водорода, представляется возможность представить механизм формирования
атомов периодической системы элементов в зависимости от атомной массы (см.
табл. 1-3).
Вместе с процессом формирования кристаллов атомов химических элементов
рассмотрим физический смысл главного понятия в химии – понятие о валентности.