115
приводит к формированию полукольца и далее кольца. Поэтому образование 3-х, 4-
х, 5-ти и 6-членных колец проходит легко.
Напомним, что выше отмечалось, что электрон в атоме Н, а это и есть
валентный диполь p
+
-ē, может занимать любое положение в сфере действия
своего протона, однако под действием внешних сил – магнитного или
электрического поля, электрон может изменить свое положение в
соответствии с направлением приложенного поля. Отсюда следует, что
валентные силы могут изменять свое направление в зависимости от
воздействия внешних сил, например, свободного валентного диполя соседней
молекулы. Устойчивость шестичленных циклических молекул можно объяснить
усилением общего силового поля многоатомных молекул по сравнению с 3-х
членными циклами, и теория Байера пусть останется в анналах научной истории в
соответствии со временем поэтапного развития научных знаний.
В нефтях обнаружены би- и трициклические нафтены. Например, декалин
С
1 0
Н
1 8
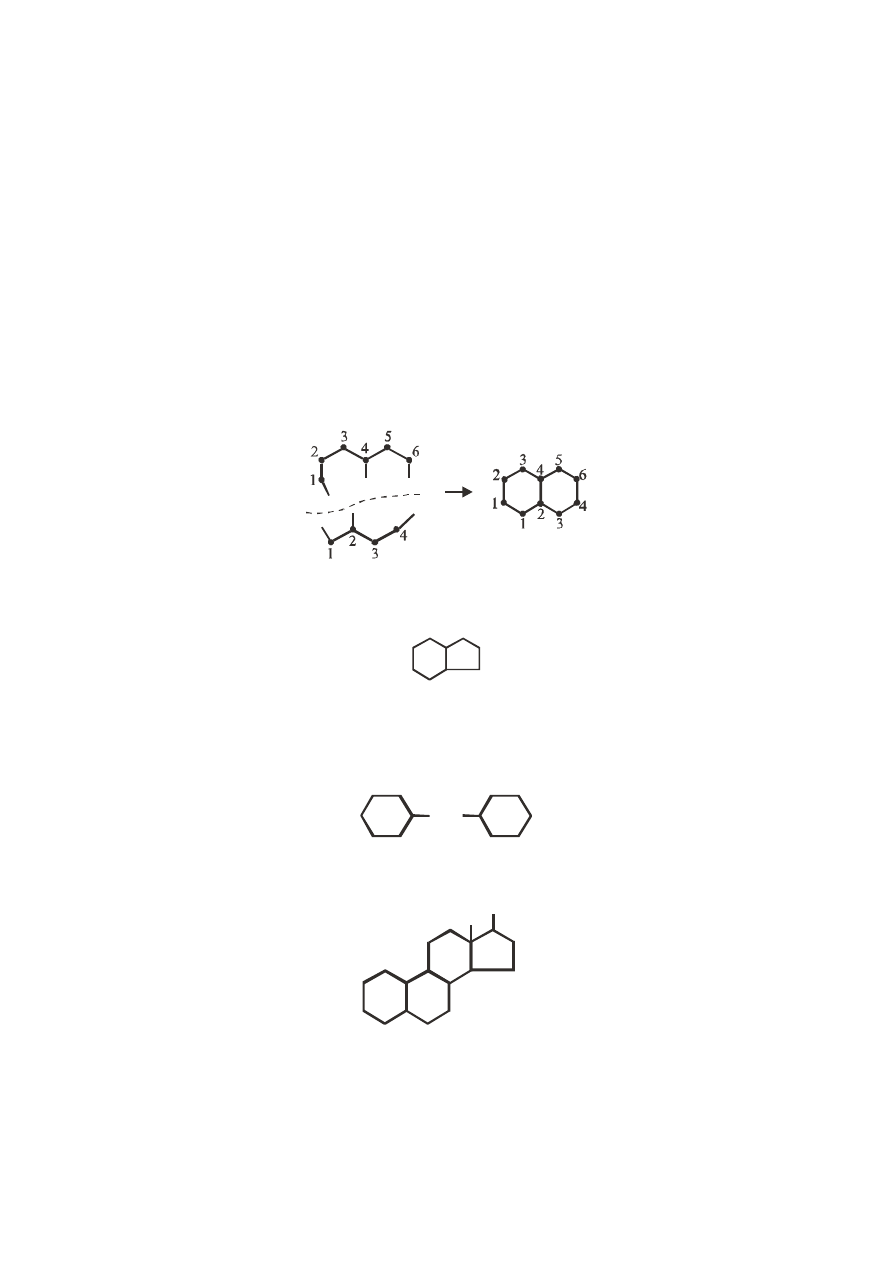
может быть образован из зигзагообразной (не плоскостной) цепочки из 6-ти
атомов С, три из которых имеют открытые валентности и такой же неплоской
цепочки из 4-х атомов С, три из них имеют также открытые валентности.
Взаимодействие двух цепей приводит к формированию двух соединенных
колец. По такой же схеме может происходить формирование сдвоенного 6-
членного и 5-членного кольца:
По такой же схеме возможно образование трехкольчатого нафтена типа
адамантана.
Метиленовая группа может сыграть роль мостика между двумя вылентно
насыщенными кольцами как в метилендициклогексане:
CH
2
Доказано присутствие в нефтях нафтеновых углеводородов с четырьмя и пятью
циклами, например, холестана:
H C
3
C H
8
17
Число атомов С боковых цепях нафтенов имеет довольно широкий диапозон от
3 до 20-28. Эти углеводороды можно относить к парафино-циклопарафиновым
углеводородам. По химическим свойствам нафтены близки к алканам. Хвосты СН
3
могли быть окислены НОН при соответствующей температуре и получены
кислотные