104
В качестве примера рассмотрим две гомогенные реакции и одну гетерогенную
с участием молекулы воды.
10.7 Участие воды в преобразованиях органических молекул.
Пример 1.
Действие воды на реакции преобразования молекул углеводородов в
гомогенной среде проявляются практически во всех типах реакций. Для примера
рассмотрим механизм реакции присоединения галогена к олефинам. В качестве
галогена возьмём молекулу Br
2
, а олефина – молекулу этилена. Реакция
записывается так:
H C = C H + Br H C C H
2
H H
H H
Br Br
Присутствие всего лишь одной молекулы воды, бесконтрольно попавшей в
реакционную смесь (как отмечалось выше, возможно из пор стекла, из которого
изготовлен реактор), позволяет легко объяснить механизм этой реакции.
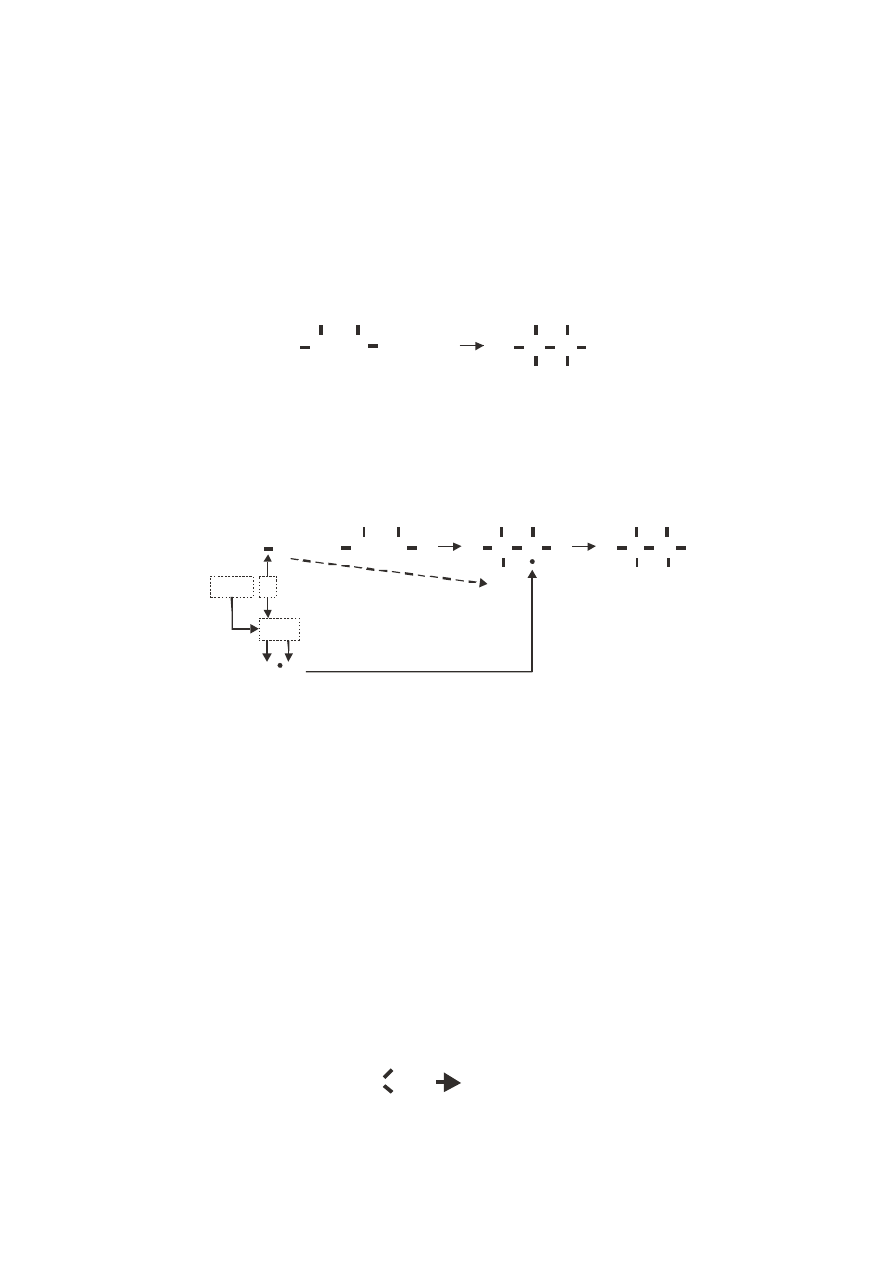
Запишем схему реакции в нашем представлении:
(Br Br) +
H C C H
H C = C H H C C H
H H
H H
Br Br
H H
Br
H
(I) OH
(-)
HBr
(I) HOH Br
Одна молекула НОН (I) в диссоциированном виде подошла к молекуле Br
2
.
Атом Н в силу своих «радикальных» свойств, описанных ранее, вторгается в связь
между атомами брома; образуется молекула HBr и атом Br
со свободным
валентным диполем (радикалом), который сразу же внедряется в двойную связь
молекулы Н
2
С=С
2
Н, разрывает её и соединяется с одним атомом углерода, образуя
связь C-Br, при этом на втором атоме С открывается свободный валентный диполь
(радикал). Затем, ранее образовавшаяся молекула HBr, подвергается атаке ОН-
группы со свойствами основания, которая взаимодействует с атомом Н молекулы
HBr, образует молекулу НОН и радикал атома Br
, который взаимодействует с
радикалом атома С
, образуя связь С-Br со вторым атомом С. В результате
сформировалась молекула дибромэтила Н
2
BrC-CBrH
2
и выделилась исходная
молекула НОН, которая сыграла роль катализатора.
Пример 2.
Рассмотрим более сложную реакцию – действие тионилхлорида на спирт,
которая имеет следующий вид:
C H OH + O = S C H Cl + HCl + SO
2
5
2
5
2
Cl
Cl