103
При дальнейшем повышении температуры кривая выделения газов снова
поднимается вверх, что объясняется выделением растворённых в стекле газов,
главным образом за счет выделения водяного пара, который образуется при
терморазложении стекла [23].
Вода является незаметным и никем не учитываемым катализатором абсолютно
всех реакций между молекулами, как в газовой, так и в жидкой среде, как для
органических, так и для неорганических молекул. Повышение температуры
реактора (энергия активации) приводит к десорбции молекул воды со(из) стенок
реактора и резкому увеличению степени диссоциации молекул воды на атом Н и
группу ОН. Появление маленького, агрессивного атома Н и его действия приводит
к образованию так называемого «переходного комплекса», а в наших
представлениях – свободного валентного диполя (радикала), хотя бы в одной из
молекул реактантов, что способствует началу любой химической реакции между
молекулами.
Рассмотрим, как происходит образование активной, реакционно-способной
молекулы в смеси двух или нескольких молекул-реактантов находящихся в
реакторе.
Наиболее реакционно-способными молекулами будут являться те, которые
имеют в своем составе атом, обладающий наибольшей величиной потенциала
ионизации (ПИ) и, имеющий свободный валентный диполь. Каков же механизм
образования свободного валентного диполя в молекуле?
Ранее в разделе 6 «О полярности связи» отмечалось, что по величине ПИ
можно качественно судить о длине валентного диполя атома; чем больше ПИ
атома, тем меньше длина валентного диполя атома р
+
-ē и наоборот.
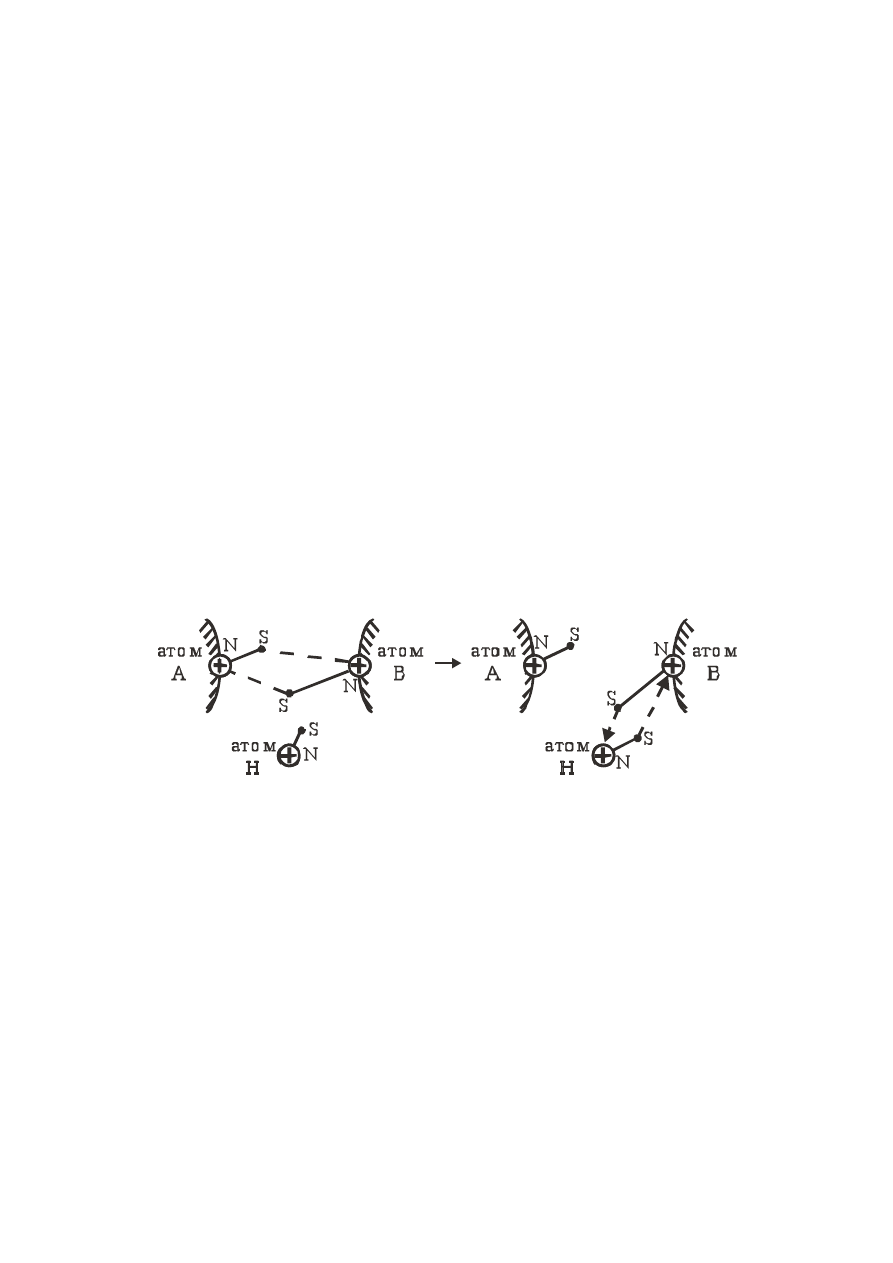
Рассмотрим, например, связь между атомами А и В. В соответствии с ПИ этих
атомов связь между атомами можно представить так:
Связь между атомами А и В осуществляется путём взаимодействия двух
валентных диполей или двух валентных магнитов – один короткий N-S у атома А,
второй – длинный N-S у атома В. Видно, что связь между атомами асимметрична.
Свободный атом Н – это элементарный магнит р
+
-ē или N-S. Известно, что полюс S
будет притягиваться к полюсу N. Приблизившись к полюсу N атома В, наиболее
сильный магнит атома Н, замыкает на себя более длинный магнит атома В.
Образуется новая связь (диамагнитная или валентная) между атомами В и Н, т.е.
связь В-Н, а магнит атома А (он же валентный диполь) становится свободным
(свободный радикал) и готовым к дальнейшим взаимодействиям со связями других
молекул. Для примеров в качестве атома А может быть использован атом N
(П.И.=14,5 эв) или атом О (П.И.=13,6 эв), а в качестве атома В можно взять атом C
(П.И.=11,3 эв).
Продолжим наши соображения относительно механизмов химических реакций.
Считаем, что для осуществления любых химических реакций необходимо
присутствие как минимум свободного атома водорода. Постоянным источником
атомов водорода является вода. Выше уже отмечалось, что растворителем веществ
или отделителем атомов друг от друга в любых соединениях является свободный
атом водорода, независимо от способа его получения.